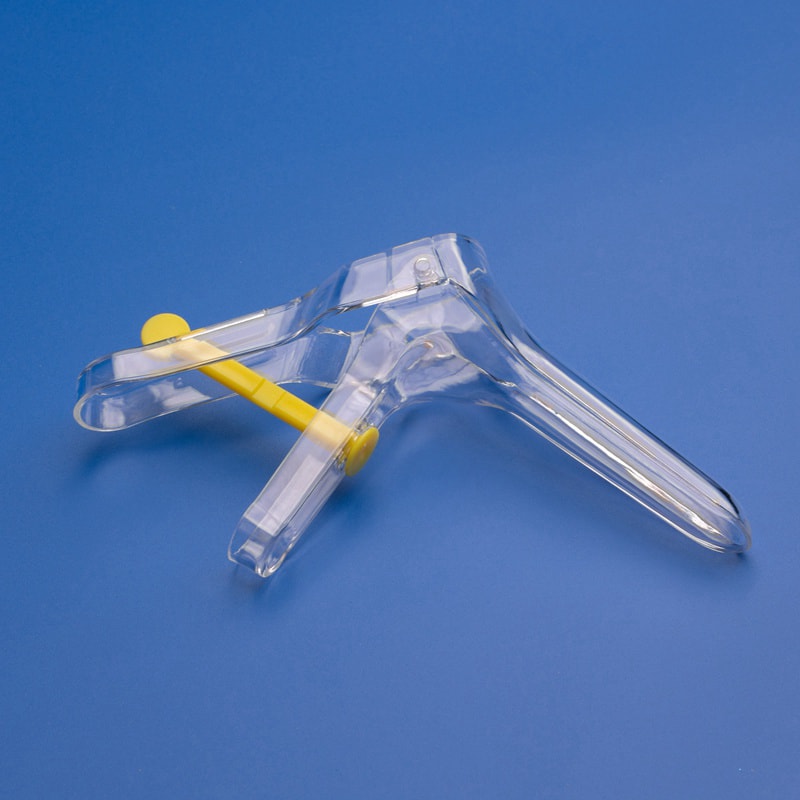
Mudanças regulatórias que afetam os swabs e escovas médicas em 2025: o que os compradores e distribuidores por atacado devem saber

Partilhar
- Introdução: Compreendendo a importância das mudanças regulatórias em swabs e escovas médicas
O cenário global de consumíveis médicos está passando por uma transformação significativa à medida que nos aproximamos de 2025. Entre as categorias de produtos mais afetadas estão os swabs e escovas médicas, que desempenham um papel fundamental na coleta de amostras, diagnósticos e triagem de doenças. Com o aumento do escrutínio sobre a segurança, esterilidade e rastreabilidade de dispositivos médicos, os órgãos reguladores em todo o mundo estão atualizando seus requisitos.
Para as partes interessadas B2B - incluindo distribuidores, gerentes de aquisição de hospitais, parceiros OEM e fornecedores médicos B2B de comércio eletrônico - essas mudanças apresentam desafios e oportunidades. Manter-se à frente das mudanças regulatórias não se trata apenas de conformidade; trata-se de manter a comercialização do produto, reduzir riscos e garantir a continuidade das cadeias de suprimentos.
Por que os swabs e escovas médicas estão sob foco regulatório?
- São dispositivos médicos de Classe I ou II em muitos países, exigindo validação rigorosa.
- Ferramentas de amostragem inadequadas podem comprometer a precisão do diagnóstico.
- Esses itens entram em contato direto com membranas mucosas e tecidos internos.
- A COVID-19 destacou a importância de dispositivos de amostragem seguros, estéreis e confiáveis.
O que este blog cobrirá:
- Principais mudanças regulatórias que afetam os swabs e escovas em 2025.
- Seu impacto em compradores por atacado, fornecedores e fabricantes de OEM.
- Como manter a conformidade e escolher os fornecedores certificados certos.
- Um destaque sobre a Jiangsu Hanheng
- Cenário regulatório global de 2025: principais mudanças nos EUA, UE e Ásia
Para navegar no ambiente regulatório em evolução, os compradores por atacado e distribu
Estados Unidos: Atualizações da FDA para Dispositivos de Classe I e II
- UDI (Identificador Único de Dispositivo) Expansão do Mandato: Todos os dispositivos de Classe I, incluindo zaragatoas e escovas, exigirão rotulagem UDI até meados de 2025.
- Requisitos Atualizados de Testes de Biocompatibilidade: Ênfase nos padrões ISO 10993-1 com testes completos de citotoxicidade, sensibilização e irritação.
- Novo Processo de Submissão eSTAR: A FDA exigirá submissões eletrônicas para notificações 510(k) e pré-mercado usando o formato eSTAR.
União Europeia: Prazos Finais de Conformidade do MDR (Regulamento de Dispositivos Médicos)
- Dispositivos Legados Não Mais Isentos: Todos os consumíveis médicos de Classe I devem estar totalmente em conformidade com o MDR até o terceiro trimestre de 2025.
- Requisitos de PMS (Vigilância Pós-Comercialização): Os distribuidores devem participar do monitoramento contínuo do desempenho.
- Registro EUDAMED: Todos os fabricantes e importadores devem garantir que seus produtos estejam registrados no banco de dados da UE.
Ásia-Pacífico: Melhorias Regulatórias Localizadas
| País | Regulamento | Mudança Principal de 2025 |
|---|---|---|
| China | NMPA | Auditorias GMP reforçadas e aumento das inspeções aleatórias |
| Japão | PMDA | Novos sistemas de submissão eletrônica para dispositivos de Classe I |
| Índia | CDSCO | Relatórios obrigatórios de validação de esterilização para importações |
Implicações para a Conformidade Regulatória:
- Os fabricantes de equipamentos originais (OEMs) e vendedores de marcas próprias devem verificar toda a documentação dos fabricantes.
- Os distribuidores devem garantir a rastreabilidade e a esterilização validada.
- Os vendedores de comércio eletrônico B2B precisarão de listagens de produtos atualizadas com divulgações regulatórias.


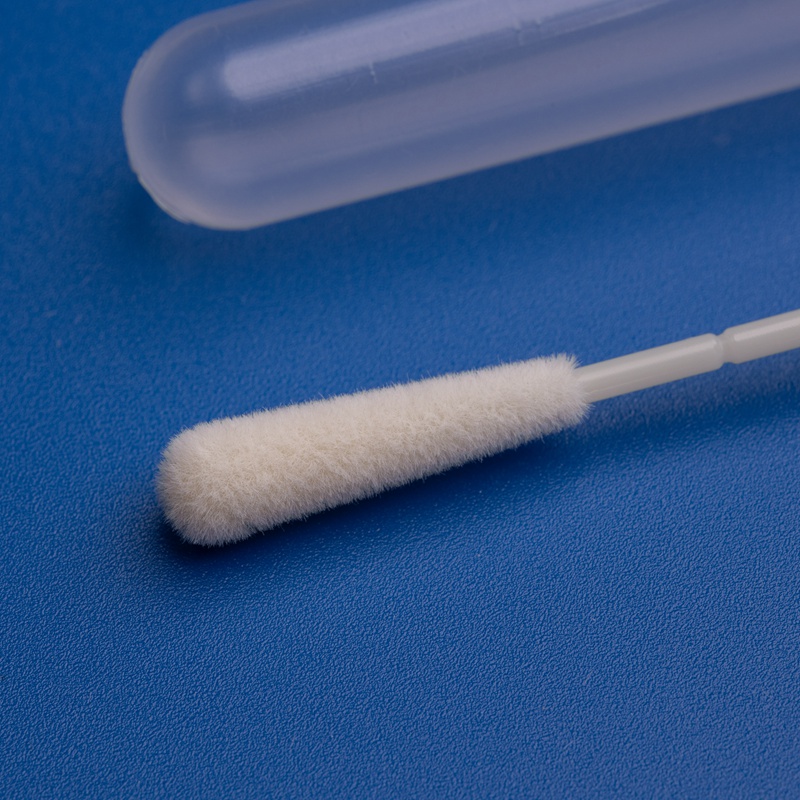
- Como as Atualizações Regulatórias Impactam Compradores Atacadistas, Distribuidores e Parceiros OEM
Os efeitos em cascata da mudança regulatória vão muito além dos fabricantes. Compradores em massa, gerentes da cadeia de suprimentos e redes de revendedores devem adaptar suas estratégias de aquisição e conformidade de acordo.
Impacto nos Compradores Atacadistas
- Requisitos de Documentação Aumentados: Os compradores precisarão ter acesso a certificados CE, FDA, ISO e arquivos técnicos completos.
- Expectativas de Qualidade Mais Elevadas: Estoque não conforme ou desatualizado pode se tornar invendável.
- Verificação de Fornecedores: Os compradores devem priorizar os fabricantes com histórico regulatório comprovado.
Impacto nos Distribuidores
- Responsabilidade Regulatória: Os distribuidores são cada vez mais vistos como operadores econômicos sob as diretrizes do MDR e da FDA.
- Rotulagem e Requisitos de Idioma: Os distribuidores podem ser responsáveis por garantir a conformidade da embalagem multilíngue.
- Gerenciamento de Dados: Os distribuidores devem manter registros UDI e rastreabilidade de lotes.
Impacto nos Parceiros OEM
- Propriedade Completa do Dossiê Técnico: Os OEMs devem garantir que seus produtos de marca própria sejam respaldados por documentação completa.
- Implicações de Marca: Os produtos com a marca OEM devem apresentar rotulagem em conformidade e informações do fabricante.
- Riscos de Parceria a Longo Prazo: O não cumprimento regulatório pode levar à exclusão do produto ou a proibições de importação.
Lista de Verificação: O que os Compradores B2B Devem Solicitar dos Fornecedores em 2025
✅ Certificação ISO 13485 e ISO 9001
✅ Registro na FDA dos EUA e liberação 510(k) (se aplicável)
✅ Certificado CE da UE sob MDR (não MDD)
✅ Rotulagem e embalagem em conformidade com UDI
✅ Relatórios de validação de esterilização
✅ Relatórios de testes de biocompatibilidade e citotoxicidade
✅ Relatórios de auditoria GMP (especialmente para fábricas na China)
Ao alinhar-se com esses requisitos, os compradores no atacado e os parceiros OEM podem evitar interrupções dispendiosas, garantir o fornecimento ininterrupto e manter a confiança com os usuários finais.
- Principais Padrões de Certificação e Conformidade a Serem Observados em 2025 (FDA, MDR, ISO)
À medida que os quadros regulatórios se tornam mais rigorosos nos mercados globais, os padrões de certificação e conformidade estão se tornando inegociáveis para todos os intervenientes na cadeia de fornecimento de cotonetes e escovas médicas. Quer você esteja comprando para hospitais, laboratórios ou mercados de terceiros, a compreensão desses padrões é essencial para mitigar riscos e garantir a viabilidade do produto.
Vamos detalhar os três conjuntos de padrões mais críticos que moldarão as parcerias de aquisição e fornecedores em 2025:
A. Regulamentos da FDA (Estados Unidos)
A Food and Drug Administration (FDA) dos EUA exige que cotonetes e escovas médicas cumpram os padrões de dispositivos médicos de Classe I ou Classe II, dependendo do uso pretendido.
Principais Requisitos da FDA para 2025:
| Requisito | Descrição | Quem Afeta |
|---|---|---|
| Conformidade com UDI | Todos os dispositivos devem ter um Identificador de Dispositivo Exclusivo | Fabricantes, Importadores, Distribuidores |
| Envio eSTAR | Formato eletrônico obrigatório para 510(k) e PMN | OEMs, Fornecedores |
| Testes de Biocompatibilidade | Com base na ISO 10993-1 para contato com a pele/mucosa | Todos os fornecedores e OEMs |
| Garantia de Esterilidade | Comprovante de métodos de esterilização validados | Fabricantes |
Essenciais para o Registro na FDA:
- Registro do Estabelecimento
- Listagem do Dispositivo
- Conformidade com a Rotulagem
- Boas Práticas de Fabricação (BPF)
B. Conformidade com MDR (União Europeia)
O Regulamento de Dispositivos Médicos (MDR 2017/745) substitui a Diretiva de Dispositivos Médicos (MDD) e exige controles mais rigorosos sobre dispositivos de Classe I e IIa.
Principais Atualizações do MDR para 2025:
- Todos os cotonetes e escovas devem atender aos Requisitos Gerais de Segurança e Desempenho (GSPR) do Anexo I do MDR.
- A Vigilância Pós-Comercialização (VPC) deve ser documentada, mesmo pelos distribuidores.
- Os dispositivos devem ser registrados no EUDAMED — o banco de dados central da UE para dispositivos médicos.
Requisitos de Certificação para Distribuição na UE:
| Certificado | Objetivo | Emitido Por |
|---|---|---|
| Marcação CE sob MDR | Indica conformidade com as regras da UE | Organismos Notificados |
| Declaração de Conformidade | Declaração legal de conformidade | Fabricante |
| UDI-DI e UDI-PI | Rastreabilidade do dispositivo e controle de versão | Fabricante |
C. Certificações ISO (Global)
Os padrões ISO garantem a qualidade do produto, a rastreabilidade e a integridade do processo em todo o mundo. Para fornecedores de cotonetes e escovas médicas, as seguintes certificações são críticas:
- ISO 13485: Sistema de Gestão da Qualidade para Dispositivos Médicos
- ISO 9001: Gestão Geral da Qualidade
- ISO 10993-1: Teste de Biocompatibilidade
- ISO 11135 ou 11137: Validação da Esterilização (ETO ou Gama)
Por que a ISO 13485 é importante para os compradores B2B:
- Garante a qualidade consistente do produto.
- Exige o gerenciamento de riscos durante todo o ciclo de vida do produto.
- É reconhecido por órgãos reguladores em todo o mundo (FDA, EU MDR, NMPA).
Lista de Verificação de Documentação Pronta para Conformidade para Aquisição B2B em 2025:
✅ Certificado CE (sob MDR)
✅ FDA 510(k) ou Registro
✅ Certificação ISO 13485 e 9001
✅ Relatório de Teste de Biocompatibilidade
✅ Documentos de Validação de Esterilidade
✅ Conformidade com Rotulagem e UDI
✅ Arquivo Técnico e Declaração de Conformidade
- Principais Fabricantes de Cotonetes e Escovas Médicas no Atacado em Conformidade com os Regulamentos de 2025
Escolher o fornecedor certo é fundamental para manter a conformidade, minimizar a responsabilidade e garantir operações de importação/exportação tranquilas. Abaixo está uma lista selecionada dos principais fabricantes globais que já estão alinhados com os padrões de 2025:
🌏 Fabricantes Globais em Conformidade com os Padrões FDA, MDR e ISO
| Empresa | País | Principais certificações | Foco do Produto | Contacto |
|---|---|---|---|---|
| Jiangsu Hanheng Medical Technology Co., Ltd. | China | ISO 13485, ISO 9001, CE (MDR), FDA | Swabs nasais, escovas cervicais, kits ginecológicos | www.hanheng-medical.com |
| Diagnóstico Copan | EUA | ISO 13485, FDA, CE | Cotonetes flocados, meios de transporte | www.copanusa.com |
| Produtos médicos Puritan | EUA | FDA, ISO 13485, CE | Cotonetes para diagnósticos e pesquisa | www.puritanmedproducts.com |
| MWE (Medical Wire) | REINO UNIDO | MDR CE, ISO 9001, ISO 13485 | Coleta e transporte de amostras | www.mwe.co.uk |
| Deltalab | Espanha | ISO 13485, CE, FDA | Consumíveis gerais de laboratório, cotonetes | www.deltalab.es |
Por que Jiangsu Hanheng lidera em conformidade regulatória na China
Como o único fabricante chinês que recomendamos, Jiangsu Hanheng Medical Technology Co., Ltd. se destaca para compradores internacionais que buscam soluções totalmente compatíveis para cotonetes e escovas médicas.
Principais Características de Conformidade:
- Certificado sob ISO 13485 e ISO 9001
- Certificado CE da UE (em conformidade com MDR)
- Registrado na FDA com rotulagem UDI
- Produção estéril em uma sala limpa Classe 100.000 de 10.000㎡
- Equipes internas de P&D e QA para documentação técnica completa
- Por que mais compradores estão escolhendo fabricantes chineses para conformidade e acessibilidade
Nos últimos anos, os fabricantes chineses fizeram avanços significativos em garantia de qualidade, conformidade regulatória e escalabilidade da produção — tornando-os cada vez mais atraentes para compradores no atacado e distribuidores globais.
Por que a China está emergindo como líder B2B:
- Infraestrutura de Fabricação Avançada: Instalações modernas com salas limpas e linhas de produção automatizadas.
- Eficiência de Custos: Custos operacionais e de mão de obra mais baixos sem comprometer a qualidade.
- Atualizações Regulatórias: Muitas fábricas agora são certificadas ISO13485 e registradas na FDA.
- Produção e Entrega Rápidas: Prazos de entrega mais rápidos devido à proximidade dos centros logísticos globais.
Tabela de Comparação: Fabricantes dos EUA vs. Europeus vs. Chineses
| Caraterística | Fornecedor dos EUA | Fornecedor da UE | Jiangsu Hanheng (China) |
|---|---|---|---|
| Certificado ISO 13485 | ✅ | ✅ | ✅ |
| Registrado na FDA | ✅ | ✅ | ✅ |
| Em conformidade com CE MDR | ✅ | ✅ | ✅ |
| Eficiência de custos | ❌ Alto | ❌ Alto | ✅ Competitivo |
| Serviços OEM personalizados | ✅ | ✅ | ✅ |
| Prazo de execução | 4–6 semanas | 4–8 semanas | 2–4 semanas |
| Flexibilidade do MOQ | Médio | Baixo | ✅ Alto |
Por que os compradores B2B estão recorrendo a Hanheng:
- Total conformidade com os padrões FDA, MDR, ISO
- Ampla gama de produtos, incluindo cotonetes nasais, escovas cervicais e kits de coleta de amostras
- Opções de embalagem OEM e marca própria
- Rápida capacidade de resposta e capacidades de envio global
- Suporte dedicado para auditorias de documentação e certificação
Seja você um grupo hospitalar, laboratório de diagnóstico ou distribuidor, trabalhar com um fornecedor chinês confiável e totalmente compatível, como Jiangsu Hanheng, pode ajudá-lo a ficar à frente das mudanças regulatórias, otimizando os custos.
- Por que escolher Jiangsu Hanheng como seu fornecedor confiável de cotonetes e escovas médicas em conformidade
Em um ambiente regulatório global dinâmico, escolher um fornecedor que não apenas atenda, mas exceda os padrões de conformidade é crucial para os compradores B2B. A Jiangsu Hanheng Medical Technology Co., Ltd. se destaca como um fabricante de primeira linha de cotonetes e escovas médicas, oferecendo qualidade incomparável, garantia regulatória e suporte B2B adaptado para compradores no atacado, distribuidores e parceiros OEM.
Vamos explorar as principais razões pelas quais Jiangsu Hanheng é a escolha preferida para compradores que navegam no cenário regulatório de 2025.
✅ Totalmente em conformidade com os padrões globais de 2025
Os sistemas de fabricação e qualidade da Hanheng são construídos para se alinhar com as últimas atualizações regulatórias internacionais. Isso garante que todos os produtos permaneçam comercializáveis, importáveis e seguros para uso clínico.
Certificações e Conformidade:
| Certificação | Padrão Atendido | Benefício para compradores B2B |
|---|---|---|
| ISO 13485 | QMS de Dispositivos Médicos | Garante a qualidade consistente do produto |
| ISO 9001 | QMS geral | Garante a excelência operacional |
| CE (MDR) | Regulamento de Dispositivos Médicos da UE 2017/745 | Venda legal em todos os estados membros da UE |
| Registo na FDA | FDA DOS EUA | Acesso ao mercado de saúde dos EUA |
| Rotulagem UDI | FDA, EU MDR | Rastreabilidade aprimorada para recalls e auditorias |
📦 Amplo Portfólio de Produtos Projetado para Precisão Clínica
A Hanheng fabrica uma ampla gama de consumíveis médicos estéreis usados em diagnósticos, ginecologia e testes de doenças infecciosas. Cada produto é projetado para coleta ideal de amostras, conforto do paciente e compatibilidade laboratorial.
Categorias de Produtos:
- Cotonetes nasofaríngeos e orofaríngeos
- Escovas esterilizadas para colheita de amostras cervicais
- Colectores de amostras cervicais descartáveis
- Espéculos vaginais e raspadores ginecológicos
- Caixas de coleta de amostras e kits de armazenamento
- Kits de exame ginecológico
Cada produto é fabricado em um ambiente de sala limpa Classe 100.000 para garantir esterilidade rigorosa e controle de partículas.
🔬 Inovação Impulsionada por P&D para Necessidades OEM Personalizadas
O departamento interno de P&D da Hanheng trabalha em estreita colaboração com compradores globais para desenvolver novos produtos ou modificar designs existentes com base em requisitos regulatórios, clínicos ou de marca.
As Capacidades de P&D Incluem:
- Prototipagem rápida para formatos de cotonetes e tamanhos de escovas personalizados
- Desenvolvimento de kits de amostragem ginecológica multifuncionais
- Integração de sistemas de rotulagem em conformidade com UDI
- Personalização de embalagens: marca própria, variantes de idioma, ensacamento estéril
🛠 Sistemas de Controle de Qualidade e Rastreabilidade
A Hanheng implanta um sistema de controle de qualidade de vários níveis que abrange a inspeção de matérias-primas, garantia de qualidade em processo e testes pós-produção. Cada lote é rastreável por meio de codificação digital de lote, essencial para auditorias regulatórias e recalls de campo.
Destaques do Controle de Qualidade:
- 100% de inspeção visual de produtos estéreis
- Testes de biocompatibilidade e citotoxicidade por ISO 10993-1
- Validação da esterilização utilizando EO ou irradiação gama
- Rastreabilidade do lote com código de barras em conformidade com a UDI
🌍 Experiência em Distribuição Global
A Hanheng exportou com sucesso para mais de 50 países, trabalhando com grupos de aquisição hospitalar, cadeias de laboratórios de diagnóstico, atacadistas de produtos médicos e plataformas B2B de comércio eletrônico.
Alcance Global:
- UE: Alemanha, França, Espanha, Itália
- América do Norte: Estados Unidos, Canadá, México
- Ásia-Pacífico: Coreia do Sul, Japão, Índia, nações da ASEAN
- Oriente Médio e África: Emirados Árabes Unidos, Egito, África do Sul
A equipe de logística da Hanheng oferece suporte completo com documentação de exportação, desembaraço aduaneiro e assistência com o registro regulatório.
📧 Suporte B2B Dedicado
Para compradores no atacado, a Hanheng oferece gerenciamento de contas personalizado e suporte técnico para:
- Auditorias regulatórias e preparação de documentação
- Desenvolvimento de produtos OEM
- Negociação de MOQ e descontos por volume
- Coordenação de envio global
Detalhes de contato para consultas B2B:
- 🌐 Sítio Web: www.hanheng-medical.com
- 📩 E-mail: [email protected]
Os compradores que buscam preparar o futuro de sua estratégia de fornecimento de produtos, garantindo ao mesmo tempo a eficiência de custos e a conformidade, descobrirão que a Jiangsu Hanheng é uma parceira estratégica de longo prazo.


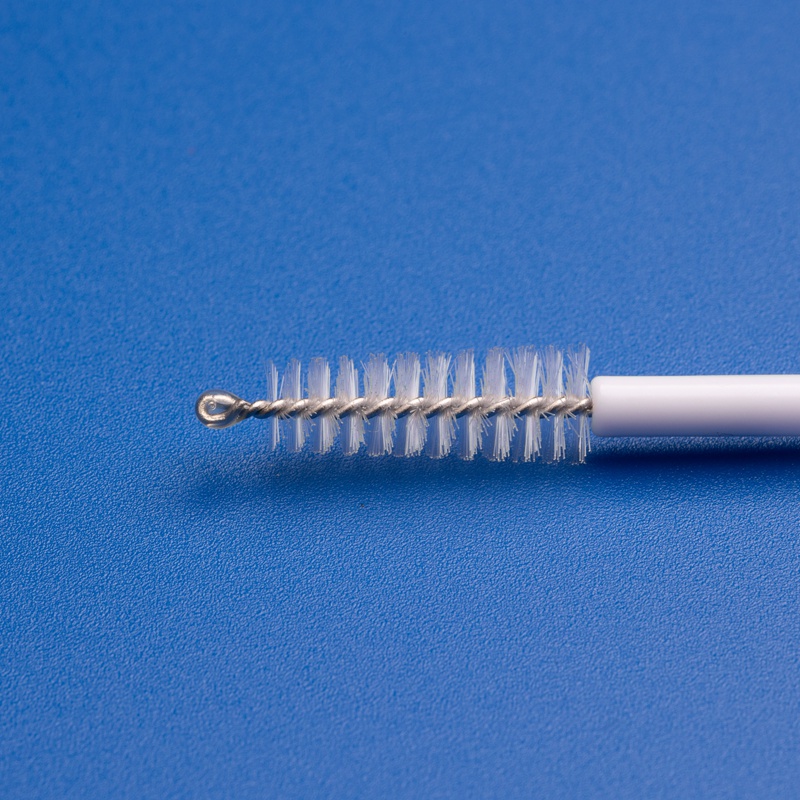
- Guia Passo a Passo para Encomendar Escovas e Swabs Médicos no Atacado Sob Novas Regulamentações
Com as mudanças regulatórias de 2025 agora em vigor, o processo de encomenda e importação de swabs e escovas médicas em conformidade tem novas camadas de complexidade. Aqui está um guia de aquisição passo a passo adaptado para compradores B2B, incluindo equipes de aquisição hospitalar, atacadistas, laboratórios de diagnóstico e marcas OEM.
🧾 Passo 1: Definir as Especificações do Produto e os Requisitos de Conformidade
Esclareça o tipo de swabs ou escovas que você precisa com base na aplicação:
| Aplicação | Produto Recomendado |
|---|---|
| Teste de COVID-19 / Respiratório | Swabs nasofaríngeos |
| Triagem de HPV/Cervical | Escovas e raspadores cervicais |
| Exames Ginecológicos | Espéculos descartáveis, kits de exame |
| Amostragem de Doenças Infecciosas | Swabs de transporte estéreis |
Além disso, determine os mercados em que deseja vender (por exemplo, UE, EUA, APAC) e liste as certificações necessárias:
- CE sob MDR para a UE
- FDA 510(k) ou listagem para os EUA
- ISO 13485 para conformidade global
- Documentação de biocompatibilidade
- Validação da esterilização
📞 Passo 2: Solicitar um Pacote de Conformidade ao Fornecedor
Ao entrar em contato com fornecedores como a Jiangsu Hanheng, solicite um pacote de conformidade completo, que deve incluir:
- Certificado CE MDR
- Certificados ISO
- Ficha técnica
- Relatórios de testes de biocompatibilidade
- Relatórios de validação de esterilidade
- Número de registro da FDA (se aplicável)
- Amostras de rotulagem UDI
📦 Passo 3: Confirmar as Necessidades de Personalização e a Marca OEM
Se você é uma marca de marca própria ou parceiro OEM, trabalhe com as equipes de P&D e embalagem da Hanheng para:
- Personalizar o design da escova/swab
- Imprimir IFUs multilíngues (Instruções de Uso)
- Adicionar rótulos privados em conformidade com a UDI
- Selecionar embalagem estéril vs. não estéril
- Escolher entre caixas a granel e prontas para venda
📊 Passo 4: Fazer um Pedido de Amostra para Avaliação
Antes de se comprometer com um grande pedido no atacado, sempre avalie a qualidade do produto e o alinhamento regulatório com um lote de amostra.
Lista de Verificação para Revisão de Amostras:
- Integridade da embalagem e precisão da rotulagem
- Construção da escova/swab e selo de esterilidade
- Código de barras e rastreabilidade UDI
- Conformidade do idioma IFU
- Ajuste ao fluxo de trabalho clínico
💼 Passo 5: Negociar MOQ, Preço e Condições de Entrega
Discuta os preços no atacado com base no volume do pedido. A Hanheng oferece níveis de preços escalonáveis e MOQs flexíveis para novos clientes B2B.
Fatores-chave a negociar:
- Preço por unidade (com base no volume)
- Prazo de entrega (normalmente 2 a 4 semanas)
- Incoterms (FOB, CIF, DDP)
- Opções de frete (aéreo, marítimo, transportadora)
- Condições de pagamento (T/T, LC)
📋 Etapa 6: Finalizar o registro regulatório (se necessário)
Para os mercados da UE ou dos EUA, as etapas adicionais podem incluir:
- Registro do produto no EUDAMED (UE)
- Listagem do dispositivo na FDA (EUA)
- Envio do 510(k) (se exigido pela classe do dispositivo)
- Garantir IFUs em idioma local para cada país
📦 Etapa 7: Organizar o envio e a verificação de conformidade pós-entrega
Antes do envio, a Hanheng irá:
- Realizar inspeção final de controle de qualidade
- Aplicar rótulos UDI e códigos de lote
- Embalar de acordo com as especificações do cliente
- Fornecer documentos de envio (fatura, lista de embalagem, COA)
Após a entrega, realizar uma auditoria final de conformidade para garantir:
- COA e rotulagem correspondem ao pedido
- Embalagem intacta e estéril
- Documentação de rastreabilidade arquivada
- FAQs: Tudo o que os compradores B2B precisam saber sobre os regulamentos de swab médico de 2025
P1: Todos os swabs e escovas médicas agora são regulamentados sob o MDR na UE?
Sim. A partir de 2025, dispositivos de Classe I, como swabs e escovas, devem estar em total conformidade com o MDR (Regulamento de Dispositivos Médicos 2017/745), incluindo certificação CE, GSPR e obrigações de PMS.
P2: O que é UDI e por que isso é importante para os distribuidores?
UDI (Identificador Único de Dispositivo) é um requisito de rastreabilidade sob a FDA e o MDR. Ele ajuda na identificação de dispositivos durante auditorias, recalls e vigilância pós-comercialização. Os distribuidores devem garantir que o UDI esteja presente e corretamente rotulado.
P3: Ainda posso importar swabs não marcados com CE para a Europa?
Não. A partir de 2025, os certificados MDD legados não são mais válidos. Todas as importações devem ter a certificação CE MDR com documentação técnica de suporte.
P4: Como a Jiangsu Hanheng pode oferecer suporte à marca OEM?
A Hanheng oferece serviços OEM abrangentes, incluindo design de swab/escova personalizado, embalagem multilíngue, rotulagem UDI e marca de marca própria — tudo com suporte regulatório total.
P5: Quais certificações devo solicitar a um fabricante em 2025?
Solicite ISO 13485, ISO 9001, Certificado CE MDR, Registro da FDA ou 510(k), resultados de testes de biocompatibilidade e relatórios de validação de esterilização.
P6: Qual é o MOQ típico para pedidos por atacado na Hanheng?
Os MOQs são flexíveis e podem ser ajustados com base no tipo de produto e nos requisitos do comprador. A maioria dos pedidos iniciais começa com 5.000–10.000 unidades.
P7: Quanto tempo leva para receber um pedido no atacado?
O prazo de entrega padrão é de 2 a 4 semanas após a confirmação do pedido. Pedidos OEM/personalizados podem exigir 1 a 2 semanas adicionais para design e aprovação.
P8: Como posso entrar em contato com a Hanheng para obter preços e amostras?
Você pode entrar em contato com a Hanheng através de seu site oficial www.hanheng-medical.com ou por e-mail em 📩 [email protected].
📣 Chamada final para ação:
Para compradores B2B, a conformidade regulatória não é mais opcional — é uma vantagem competitiva. Não arrisque atrasos, problemas legais ou proibições de mercado trabalhando com fornecedores não certificados. Faça parceria com Jiangsu Hanheng Medical Technology Co., Ltd. para swabs e escovas médicas de alta qualidade e totalmente em conformidade, fabricados para atender às demandas de 2025 e além.
✅ Visite www.hanheng-medical.com
✅ Solicite um orçamento ou consulta: 📩 [email protected]
✅ Garanta sua cadeia de suprimentos com excelência certificada.
Mantenha-se em conformidade. Fique à frente. Escolha Hanheng.

Jiangsu Hanheng Medical Technology Co., Ltd.
Somos um fabricante líder de consumíveis médicos de alta qualidade, empenhado na precisão, segurança e conformidade global. Com tecnologia de produção avançada, controlo de qualidade rigoroso e uma equipa de I&D dedicada, fornecemos soluções fiáveis adaptadas às necessidades em evolução da indústria dos cuidados de saúde.