التنقل في لوائح الاستيراد للمسحات الطبية إلى الاتحاد الأوروبي (2025)

شارك
1. المقدمة: لماذا يهم فهم لوائح استيراد الاتحاد الأوروبي للمسحات الطبية في عام 2025
مع تشديد الاتحاد الأوروبي لمتطلباته التنظيمية الخاصة بالأجهزة الطبية والمواد الاستهلاكية التشخيصية، أصبح التنقل في لوائح الاستيراد للمسحات الطبية أولوية حاسمة للمشترين التجاريين، والموزعين، ومديري التوريد. في عام 2025، لم يعد الامتثال اختياريًا—بل هو جانب إلزامي لإجراء الأعمال عبر دول الاتحاد الأوروبي الأعضاء.
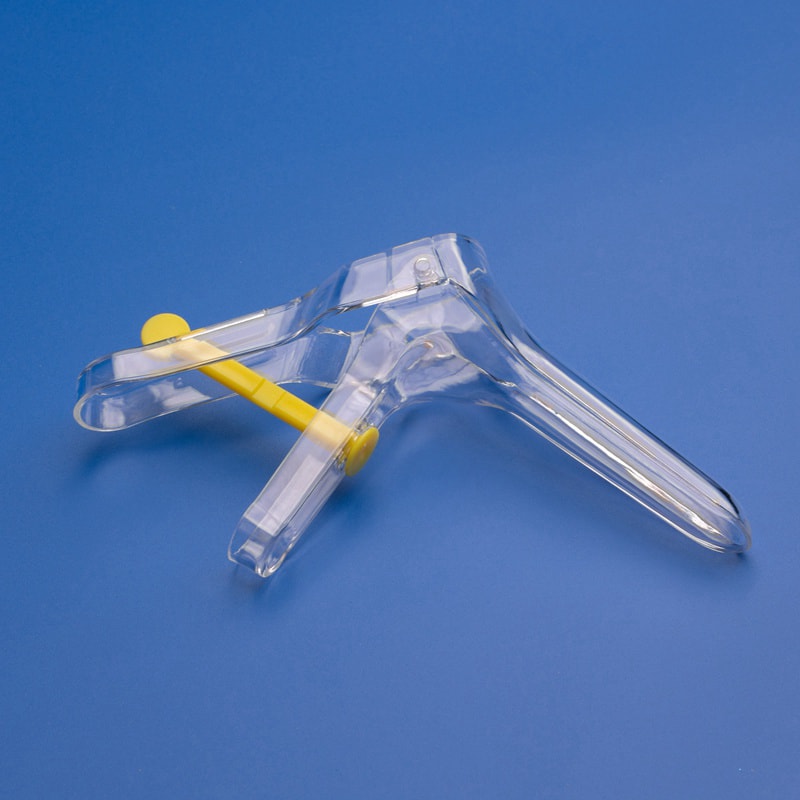
تُصنف المسحات الطبية، خاصة تلك المستخدمة في الاختبارات التشخيصية (مثل أخذ العينات الأنفية الحلقية، أو الفموية الحلقية، أو الرحمية)، كأجهزة طبية بموجب لائحة الأجهزة الطبية في الاتحاد الأوروبي (MDR 2017/745). سواء كنت تاجرًا جملة، أو موردًا للمختبرات، أو مسؤول توريد في المستشفيات، فإن ضمان توافق المنتجات المستوردة مع معايير الاتحاد الأوروبي أمر أساسي للوصول إلى السوق والتشغيل القانوني.
أهمية التوافق التنظيمي للمشترين التجاريين
- يضمن سلسلة توريد مستمرة وإفراج جمركي سلس
- يمنع التأخيرات المكلفة والغرامات أو استدعاء المنتجات
- يبني الثقة مع مقدمي الرعاية الصحية والمشترين المؤسسيين
- يعزز مصداقية العلامة التجارية واستدامة الأعمال في الاتحاد الأوروبي
الأولويات التنظيمية لعام 2025
| المجال الرئيسي | الوصف |
|---|---|
| الامتثال لـ MDR | يجب أن تتوافق جميع الأجهزة الطبية من الفئة I-III، بما في ذلك المسحات، مع MDR 2017/745 |
| علامة CE | إلزامي للوصول إلى السوق الأوروبية—يظهر تقييم التوافق |
| UDI (هوية الجهاز الفريدة) | مطلوب للتتبع والمراقبة بعد السوق |
| الممثل المعتمد للاتحاد الأوروبي | يجب على الشركات المصنعة غير الأوروبية تعيين واحد للاتصالات التنظيمية |
| التزامات المستوردين | يجب على المستوردين التحقق من الوثائق وتوافق المنتج |
فهم هذه المكونات الأساسية للبيئة التنظيمية في الاتحاد الأوروبي هو الخطوة الأولى لبناء سلسلة توريد مسحات طبية متوافقة ومربحة في عام 2025.
2. المشهد السوقي الحالي في الاتحاد الأوروبي للمسحات الطبية والمستلزمات التشخيصية
شهد سوق المسحات الطبية في الاتحاد الأوروبي نموًا كبيرًا، مدفوعًا بزيادة الطلب على اختبارات الأمراض المعدية، سرطان عنق الرحم والفحوصات، والتشخيصات الروتينية. بعد جائحة كوفيد-19، بقيت الوعي والبنية التحتية للاختبارات التشخيصية قوية، مما يخلق طلبًا مستمرًا على مسحات عالية الجودة والمواد الاستهلاكية ذات الصلة.
نظرة عامة على السوق وعوامل النمو
| العامل | التأثير على طلب المسحات |
|---|---|
| المراقبة الروتينية لكوفيد-19 | يحافظ على الطلب على المسحات الأنفية والحلقية |
| فحص HPV وسرطان عنق الرحم | يزيد من استخدام فرش الرحم والكشاطات |
| التوسع في الاختبارات في نقطة الرعاية | يتطلب أدوات أخذ عينات معقمة عالية الجودة |
| رقمنة الرعاية الصحية في الاتحاد الأوروبي | تفضل الأجهزة الطبية القابلة للتتبع والمعلمة بـ CE |
| شيخوخة السكان | يدفع الطلب على التشخيصات والفحوصات الوقائية |
الفرص المتاحة للمشترين والموزعين بين الشركات (B2B)
- المستشفيات ومختبرات التشخيص تبحث عن شركاء توريد موثوقين
- الخدمات الصحية الوطنية تسعى لتوطين التوريد
- المنصات الطبية الإلكترونية توسع نطاقها إلى المنتجات المنظمة
- منظمات البحث التعاقدية (CROs) وموردي التجارب السريرية
يمكن للموزعين التجاريين وبائعي التجارة الإلكترونية الذين يتوافقون مع التوقعات التنظيمية والجودية اختراق قطاعات الرعاية الصحية الأوروبية المربحة باستراتيجيات التوريد المناسبة.
أنواع المسحات المطلوبة بشدة في الاتحاد الأوروبي
| نوع المسحة | التطبيق | الفئة التنظيمية |
|---|---|---|
| المسحات البلعومية الأنفية البلعومية | كشف فيروسات الجهاز التنفسي | الفئة الأولى |
| مسحات البلعوم الأنفي | اختبار كوفيد-19 والإنفلونزا | الفئة الأولى |
| فرش أخذ عينات عنق الرحم | فحص فيروس الورم الحليمي البشري، مسحات عنق الرحم | الفئة الثانية أ |
| كاشطات أمراض النساء | علم الخلايا وجمع العينات | الفئة الثانية أ |
| المسحات الزغبية | اختبار المستضد/الأجسام المضادة السريع | الفئة الأولى |
أصبحت المسحات الطبية الآن أدوات أساسية في تدفقات العمل التشخيصية الأوروبية، وفهم تصنيفها بموجب MDR يساعد الموردين على استهداف القطاعات الرأسية المناسبة.



3. الإطارات التنظيمية الرئيسية في الاتحاد الأوروبي: MDR، وضع علامة CE، والامتثال الجمركي
حلت لائحة الأجهزة الطبية في الاتحاد الأوروبي (MDR 2017/745) محل اللائحة السابقة MDD بالكامل في مايو 2021، وهي الآن الإطار التنظيمي المركزي الذي يحكم استيراد وتوزيع المسحات الطبية في الاتحاد الأوروبي.
لائحة الأجهزة الطبية (MDR 2017/745)
تصنف MDR المسحات الطبية كأجهزة طبية بناءً على الاستخدام المقصود. على سبيل المثال:
- قد تكون المسحات ذات الغرض العام معفاة
- المسحات التشخيصية (الأنفية، الرحمية) عادةً من الفئة I أو IIa
- قد تكون للمسحات لأخذ العينات الذاتية متطلبات إضافية
المتطلبات الرئيسية لـ MDR للمسحات الطبية
- تصنيف المخاطر (الفئة I، IIa)
- التقييم السريري ووثائق التقنية
- خطة المراقبة بعد التسويق
- تحديد الجهاز الفريد (UDI)
- وضع علامة CE وإعلان الامتثال
وضع علامة CE للمسحات الطبية
تعتبر علامة CE علامة امتثال إلزامية للمنتجات المباعة ضمن المنطقة الاقتصادية الأوروبية (EEA). بالنسبة للمسحات الطبية، فإنها تشير إلى أن المنتج يلبي المتطلبات الأساسية للسلامة والأداء.
الخطوات للحصول على علامة CE
- تحديد تصنيف المسحة الصحيح
- تجميع ملف تقني يشمل تقييمات المخاطر وتقارير الاختبارات
- إجراء التقييم السريري (إذا كان ذلك قابلاً للتطبيق)
- تعيين ممثل مصرح له في الاتحاد الأوروبي (إذا كان الشركة المصنعة خارج الاتحاد الأوروبي)
- خضوع تقييم الامتثال (التصديق الذاتي للفئة I، هيئة إخطار للفئة IIa)
- تسجيل المنتج في قاعدة بيانات EUDAMED (قاعدة بيانات الأجهزة الطبية في الاتحاد الأوروبي)
- وضع علامة CE بشكل واضح على التغليف والوثائق
الامتثال الجمركي والاستيراد
بالإضافة إلى المتطلبات الخاصة بـ MDR، يجب على المستوردين الامتثال لإجراءات الجمارك الأوروبية، بما في ذلك:
- رموز TARIC للتصنيف الجمركي الصحيح
- إثبات الامتثال لـ CE عند الحدود
- إعلانات ضريبة القيمة المضافة للاستيراد والرسوم الجمركية
- رقم تسجيل وتحديد المشغل الاقتصادي في الاتحاد الأوروبي (EORI)
- توحيد الوثائق مع السلطات الجمركية والصحية
| عنصر الامتثال | مطلوب لـ | الجهة المسؤولة |
|---|---|---|
| علامة CE | البيع القانوني في الاتحاد الأوروبي | الشركة المصنعة |
| رقم EORI | الإفراج الجمركي | المستورد |
| ملف فني | مراقبة السوق | الشركة المصنعة |
| الممثل المصرح له | التواصل التنظيمي | الشركة المصنعة خارج الاتحاد الأوروبي |
| التسمية بلغة الاتحاد الأوروبي | تغليف المنتج | الشركة المصنعة/المستورد |
عدم الامتثال لأي من هذه المتطلبات قد يؤدي إلى رفض الجمارك أو غرامات أو مصادرة المنتج—مما يجعل التوافق التنظيمي الشامل ضرورياً لكل شحنة متجهة إلى الاتحاد الأوروبي.
4. الاعتبارات الرئيسية عند توريد المسحات الطبية للتوزيع في الاتحاد الأوروبي
اختيار المورد المناسب للمسحات الطبية يتجاوز مجرد العثور على أسعار تنافسية—إنه يتعلق بضمان الامتثال التنظيمي الكامل وجودة المنتج المتسقة والموثوقية طويلة الأمد. هذه الاعتبارات حيوية بشكل خاص عند التحضير للاستيراد إلى الاتحاد الأوروبي، حيث يتم تطبيق الامتثال لـ MDR وعلامة CE بصرامة.
العوامل الرئيسية التي يجب على الموزعين والمشترين في الاتحاد الأوروبي تقييمها
| الاعتبار | الأهمية | التأثير |
|---|---|---|
| الامتثال لـ MDR و CE | إلزامي | يضمن الوصول القانوني إلى السوق الأوروبية |
| جودة المنتج وتعقيمه | مرتفع | يؤثر على دقة التشخيص |
| تصنيع الغرف النظيفة | ضروري | يمنع التلوث |
| الشهادات (ISO، FDA، CE) | مرتفع | تثبت الثقة العالمية |
| استعداد الوثائق | مرتفع | يسهل إجراءات الجمارك |
| قابلية التوسع في التوريد | متوسط | يدعم الطلب المتزايد |
| تنوع المنتج | متوسط | يمكن من تقديم عرض أوسع للكتالوج |
جودة المنتج ومعايير العقم وجودة المنتج
يجب أن تُصنع المسحات الطبية المستخدمة في التطبيقات التشخيصية في بيئات خاضعة للرقابة لضمان عدم حدوث تلوث متقاطع أو نتائج مخنثة.
ابحث عن:
- شهادة غرفة نظيفة من الفئة 100,000 (ISO 8)
- طرق التعقيم بأكسيد الإيثيلين (EO)
- دراسات التحقق من صلاحية الصلاحية
- اختبار التوافق البيولوجي والسمية الخلوية
- تتبع الدفعة والتحكم في الدفعات
حزمة وثائق المورد للاستيراد إلى الاتحاد الأوروبي
يجب أن تشمل كل شحنة حزمة وثائق تلبي متطلبات MDR والامتثال الجمركي:
- إعلان المطابقة (DoC)
- شهادة CE (إذا كانت الفئة IIa أو أعلى)
- شهادة ISO13485
- تقرير التعقيم
- تعليمات الاستخدام (IFU) بلغات الاتحاد الأوروبي
- الملف الفني (إذا طُلب من قبل السلطة)
- UDI (معرف الجهاز الفريد)
أسئلة لطرحها على المورد الخاص بك
- هل لديك مسحات معتمدة بـ CE تلبي MDR 2017/745؟
- هل يمكنك تقديم الوثائق الفنية الكاملة للجمارك؟
- ما هي عمليات التعقيم التي تستخدمونها؟
- هل منشآتكم معتمدة بـ ISO13485؟
- هل تدعمون التسمية الخاصة أو OEM لأسواق الاتحاد الأوروبي؟
من خلال تقييم الموردين على هذه المعايير، يمكن لموزعي الاتحاد الأوروبي ومشتري B2B تقليل المخاطر التنظيمية وبناء سلسلة توريد أكثر مرونة.
5. مصنعو المسحات الطبية العالميون الموثوقون – لماذا يتصدر Hanheng من الصين
بينما يقدم العديد من المصنعين العالميين مسحات طبية، إلا أن القليل جداً يلبي احتياجات الامتثال الشامل والجودة وقابلية التوسع لسوق أوروبا. بالنسبة للمشترين المركزين على الاتحاد الأوروبي، Jiangsu Hanheng Medical Technology Co., Ltd. يبرز كأبرز مصنع صيني للمواد الاستهلاكية الطبية عالية الجودة المتوافقة مع الاتحاد الأوروبي للاختبارات الطبية.
لماذا Hanheng هو الشركة المصنعة الرائدة للمسحات الطبية في الصين
تأسست في عام 2018، وتتخصص Jiangsu Hanheng في البحث والتطوير والتصنيع للمواد الاستهلاكية التشخيصية الطبية للأسواق العالمية. مع غرفة نظيفة ISO Class 100,000 بمساحة 10,000㎡ ومجمع تصنيع يغطي 32 فداناً، تم تصميم Hanheng للإنتاج النظيف واسع النطاق الذي يلبي متطلبات الاستيراد إلى الاتحاد الأوروبي.
نطاق منتجات Hanheng لأسواق الاتحاد الأوروبي
| المنتج | التطبيق الطبي | معتمد بـ CE | فئة MDR |
|---|---|---|---|
| مسحات الأنف | اختبارات COVID-19، الإنفلونزا، RSV | ✔️ | الفئة الأولى |
| مسحات الحلق | أخذ عينات الجهاز التنفسي | ✔️ | الفئة الأولى |
| فرش عنق الرحم | فحص HPV، علم الخلايا | ✔️ | الفئة الثانية أ |
| كاشطات أمراض النساء | جمع عينات عنق الرحم | ✔️ | الفئة الثانية أ |
| جامعي عينات عنق الرحم | مسحات عنق الرحم، فيروس الورم الحليمي البشري | ✔️ | الفئة الثانية أ |
| صناديق أخذ العينات | النقل والحفظ | ✔️ | الفئة الأولى |
يتم تصنيع جميع المنتجات تحت أنظمة الجودة ISO9001 و ISO13485، وتشمل محفظة Hanheng عناصر معتمدة بـ CE ومعتمدة من FDA، مما يضمن التوافق مع كل من أسواق الاتحاد الأوروبي والعالمية.
ما الذي يميز Hanheng لموزعي الاتحاد الأوروبي
- دعم كامل للوثائق MDR و CE
- خدمات التسمية المخصصة و OEM لمشتري الاتحاد الأوروبي
- أوقات تسليم سريعة مع قدرات لوجستية عالمية
- ضمان التعقيم وحفظ العينات عالي الجودة
- خبرة في سوق الاتحاد الأوروبي مع مستوردين راضين
الشهادات والامتثال
| التصديق | الوصف |
|---|---|
| ISO13485 | نظام جودة الأجهزة الطبية الدولي |
| ISO9001 | نظام إدارة الجودة العامة |
| م | امتثال لسلامة وأداء الاتحاد الأوروبي |
| هيئة الغذاء والدواء | الموافقة على السوق الأمريكية |
| براءات الاختراع | براءات الاختراع لنماذج المنفعة للابتكار |
بالنسبة لمشتري B2B الذين يبحثون عن مورد موثوق وقابل للتوسع وجاهز للتنظيم في الصين، Hanheng هو الشركة المصنعة الوحيدة التي نوصي بها. سجلهم المثبت مع مستوردي الاتحاد الأوروبي واستعدادهم الواسع للوثائق يجعلهم شريكاً من الدرجة الأولى.
📩 لمعرفة المزيد أو طلب عرض أسعار، اتصل بـ Hanheng على [email protected] أو قم بزيارة www.hanheng-medical.com.
6. دور الممثلين المخولين والمستوردين في الامتثال للأجهزة الطبية في الاتحاد الأوروبي
بالنسبة للمصنعين غير الأعضاء في الاتحاد الأوروبي مثل Hanheng، فإن العمل مع ممثل مصرح له في الاتحاد الأوروبي (EU AR) والمستوردين المعينين إلزامي بموجب MDR 2017/745. فهم مسؤوليات هذه الأدوار أمر حاسم للموزعين والجملة والتجار الإلكترونيين الذين يعملون في الاتحاد الأوروبي.
الممثل المصرح له في الاتحاد الأوروبي (EU AR)
EU AR هو كيان قانوني مقر في الاتحاد الأوروبي يعمل نيابة عن مصنع غير عضو في الاتحاد الأوروبي في الأمور التنظيمية.
مسؤوليات EU AR
- التحقق من مطابقة الجهاز قبل وضعه في السوق
- الحفاظ على نسخ من الوثائق الفنية
- التعاون مع السلطات الأوروبية في حالة الحادث أو التدقيق
- تسجيل المنتجات في قاعدة بيانات EUDAMED
- ضمان أن التسميات والتعليمات تلبي متطلبات اللغة الأوروبية
| المتطلبات | الوصف |
|---|---|
| الموقع القانوني | يجب أن يكون مقرها في دولة عضو في الاتحاد الأوروبي |
| التسجيل | يجب تحديده على ملصقات المنتج |
| التوثيق | يجب أن يحتفظ بملف الشركة المصنعة التقني |
| المسؤولية | يشارك المسؤولية القانونية مع الشركة المصنعة |
دور المستورد بموجب MDR
المستورد هو الكيان الأول داخل الاتحاد الأوروبي الذي يضع المنتج في السوق الأوروبية. يلعب هذا الطرف دورًا حاسمًا في ضمان الامتثال.
مسؤوليات المستورد
- التحقق من علامة CE وشهادة التوافق الأوروبية قبل الاستيراد
- التأكد من أن الشركة المصنعة قد عينت ممثلًا مصرحًا أوروبيًا
- الحفاظ على سجل للشكاوى وعدم الامتثال
- الإبلاغ عن الحوادث الخطيرة إلى الشركة المصنعة والممثل المصرح
- التحقق من أن UDI مثبت ومسجل
| المهمة | يجب على المستورد... |
|---|---|
| التحقق من الملصقات | التأكد من أن الملصقات تلبي متطلبات MDR |
| تأكيد CE | التأكيد على أن المنتج يحمل علامة CE صالحة |
| الإبلاغ عن الحوادث | إخطار الممثل المصرح والجهات المختصة |
| حفظ السجلات | الحفاظ على سجل التدقيق لمدة 10 سنوات |
اختيار شركاء موثوقين
للمشترين والموزعين B2B:
- العمل مع مصنعين مثل هانهنغ الذين يفهمون بروتوكولات الممثل الأوروبي والمستورد
- التأكد من أن شريك اللوجستيات لديه معرفة بتوثيق الاستيراد MDR
- النظر في العمل مع وكلاء استيراد خدمات كاملة يقدمون AR والاستيراد تحت مظلة واحدة
💼 نصيحة مهنية: هانهينج تدعم موزعيها من خلال إعداد التوثيق الكامل MDR ويمكنها التوصية بشركاء AR أوروبيين ذوي خبرة في التعامل مع المواد الطبية الاستهلاكية.
فهم هذه الأدوار ليس مجرد تنظيمي—إنه استراتيجي. اختيار شركاء ملتزمين يضمن إفراج جمركي أسرع، ومشكلات ما بعد السوق أقل، وتوسع أكثر سلاسة عبر أسواق الاتحاد الأوروبي.
7. كيفية استيراد مسحات طبية ناجحة إلى الاتحاد الأوروبي: دليل خطوة بخطوة للموزعين
بالنسبة للمشترين B2B والمستوردين والموزعين، فإن فهم العملية من البداية إلى النهاية لاستيراد المسحات الطبية إلى الاتحاد الأوروبي أمر حاسم لضمان الامتثال وتجنب المشكلات التنظيمية أو الجمركية المكلفة. يغطي التحليل التدريجي التالي كل ما تحتاج إلى معرفته للاستيراد بنجاح في عام 2025، بموجب MDR 2017/745.
عملية الاستيراد خطوة بخطوة للمسحات الطبية إلى الاتحاد الأوروبي
| الخطوة | الوصف | الجهة المسؤولة |
|---|---|---|
| 1. تصنيف المنتج | تحديد فئة الجهاز MDR (مثل، الفئة I، IIa) | الشركة المصنعة |
| 2. علامة CE | التأكد من أن المنتج يتوافق مع CE | الشركة المصنعة |
| 3. تعيين ممثل مصرح أوروبي | مطلوب إذا كانت الشركة المصنعة خارج الاتحاد الأوروبي | الشركة المصنعة |
| 4. اختيار مستورد | كيان قانوني يضع الجهاز في السوق | موزع أو شريك لوجستي |
| 5. التحقق من التوثيق | DoC، شهادة CE، IFU، UDI، التسمية | المستورد |
| 6. التسجيل في EUDAMED | تسجيل الجهاز والجهات الاقتصادية | الشركة المصنعة/الممثل الأوروبي المصرح |
| 7. الإعلان الجمركي | رمز TARIC، ضريبة القيمة المضافة، الرسوم، التحقق من CE | المستورد/وسيط الجمارك |
| 8. الرصد بعد السوق | التعامل مع الشكاوى، الإبلاغ عن الحوادث | المستورد وممثل الاتحاد الأوروبي المعتمد |
دعونا نفكك كل من هذه الخطوات بالتفصيل أكثر.
1. تحديد تصنيف المنتج بموجب اللائحة MDR
تُصنف مسحات الطبية المستخدمة لأغراض التشخيص أو أخذ العينات عادةً كالتالي:
- الفئة I: مسحات أنفية أو حلقية
- الفئة IIa: فرشاة عنق الرحم، كشاطات النساء والتوليد، جامع عينات عنق الرحم
يحدد هذا التصنيف مستوى التدقيق التنظيمي وما إذا كان هناك حاجة إلى هيئة معتمدة لتقييم الامتثال.
2. ضمان وضع علامة CE والتوثيق الفني
يجب على الشركة المصنعة إعداد وصيانة:
- إعلان المطابقة (DoC)
- شهادة CE (إذا كانت قابلة للتطبيق)
- التوثيق الفني (الملحق II وIII من اللائحة MDR)
- تقرير التقييم السريري
- ملف إدارة المخاطر
- التحقق من التعقيم (إذا كان قابلاً للتطبيق)
مع مسحات هانهنغ المعتمدة بعلامة CE، يمكن للموزعين أن يكونوا واثقين من توافر جميع التوثيق أعلاه وامتثاله.
3. تعيين ممثل معتمد في الاتحاد الأوروبي
يجب أن تظهر تفاصيل الاتصال بممثل الاتحاد الأوروبي على ملصقات المنتج وتعليمات الاستخدام. اختر ممثلاً لديه خبرة في الأجهزة الطبية وتواصل قوي مع السلطات المختصة في الاتحاد الأوروبي.
💡 نصيحة: يمكن لهانهنغ التوصية بممثلين معتمدين في الاتحاد الأوروبي موثوقين على دراية بخطوط منتجاتها بالفعل.
4. اختيار مستورد
يصبح المستورد النقطة الأولى للاتصال مع السلطات التنظيمية بعد دخول المنتج إلى سوق الاتحاد الأوروبي. يمكنك التصرف كمستورد لنفسك أو العمل مع شريك لوجستي.
تشمل متطلبات المستورد:
- التحقق من CE وشهادة الإعلان عن الامتثال قبل الإصدار إلى السوق
- التسجيل في EUDAMED إذا لم يكن مسجلاً بالفعل
- الحفاظ على سجل الشكاوى والاستدعاءات
- الإبلاغ عن الحوادث الخطيرة
5. التحقق من توثيق المنتج قبل الشحن
قبل الاستيراد، يجب مراجعة الوثائق التالية:
- شهادة CE أو التصديق الذاتي للفئة I
- شهادة الإعلان عن الامتثال باللغة الأوروبية المناسبة
- التسمية مع UDI وعنوان ممثل الاتحاد الأوروبي والمستورد
- تعليمات الاستخدام (IFU)
- شهادات ISO13485 و ISO9001
- تقارير التعقيم والتوافق الحيوي
6. التسجيل في EUDAMED
تتطلب قاعدة بيانات الأجهزة الطبية الأوروبية (EUDAMED):
- تسجيل UDI-DI الأساسي
- تسجيل المشغل الاقتصادي (SRN)
- تسجيل الجهاز
- اليقظة والمراقبة بعد السوق
أصبح تسجيل EUDAMED إلزامياً بشكل متزايد لجميع الأجهزة من الفئة I فما فوق.
7. تصريف الجمارك في الاتحاد الأوروبي
يتطلب تصريف الجمارك:
- رقم EORI (تسجيل وتحديد المشغل الاقتصادي)
- رمز TARIC (مثل 3822.00.00 للمستحضرات التشخيصية)
- إثبات الامتثال لـ CE
- الفاتورة التجارية
- بوليصة الشحن أو AWB
- قائمة التعبئة
- دفع ضريبة القيمة المضافة الاستيرادية والرسوم الجمركية المطبقة
💡 رمز TARIC للمسحات التعقيم: 3005.90.10 (للاستخدام الطبي)
8. الحفاظ على الامتثال بعد السوق
بمجرد الاستيراد، لديك التزامات مستمرة:
- الحفاظ على قابلية تتبع المنتج
- الإبلاغ عن الحوادث للشركة المصنعة وممثل الاتحاد الأوروبي
- الرد على استفسارات السلطة المختصة
- إدارة الاستدعاءات أو الإجراءات التصحيحية للسلامة الميدانية إذا لزم الأمر
باتباع هذا الدليل الشامل للدورة الكاملة، يمكن للمستوردين والموزعين المقيمين في الاتحاد الأوروبي تبسيط عملية الامتثال الخاصة بهم وبناء سلسلة توريد موثوقة وقابلة للتوسع للمسحات الطبية.

8. التحديات الشائعة وكيفية تجنب الفخاخ التنظيمية في عام 2025
قد يبدو استيراد المسحات الطبية إلى الاتحاد الأوروبي أمراً بسيطاً، لكن العديد من الموزعين والجملة يواجهون أخطاء يمكن تجنبها تؤدي إلى تأخير الشحنات أو غرامات أو إلحاق الضرر بسمعتهم لدى الجهات التنظيمية. فهم الأخطاء الشائعة الأكثر شيوعاً—وكيفية تجنبها—يمكن أن يوفر الوقت والمال والسمعة.
أبرز 6 أخطاء امتثال عند استيراد المسحات الطبية
| الخطأ | المخاطر | كيفية التجنب |
|---|---|---|
| عدم وجود علامة CE أو عدم صحتها | مصادرة المنتج، غرامات | الشراء فقط من مصنعين متوافقين مع CE مثل هانهنغ |
| عدم تعيين ممثل مصرح له في الاتحاد الأوروبي | رفض الجمارك | تعيين ممثل مصرح له قبل الشحن |
| تصنيف المنتج غير الصحيح | فشل التدقيق، حظر السوق | التحقق من تصنيف MDR مع الشركة المصنعة |
| وثائق فنية غير كاملة | تأخيرات في الجمارك أو الرقابة | طلب الوثائق الكاملة قبل تقديم الطلب |
| وضع التسميات بلغة غير أوروبية | عدم الامتثال | التأكد من ترجمة التسميات وتعليمات الاستخدام |
| عدم وجود UDI على العبوة | عقوبة تنظيمية | التأكيد على أن الشركة المصنعة قد وضعت UDI |
التحديات الواقعية في الاستيراد
- احتجزت جمارك ألمانيا 5000 مسحة عنق الرحم لدى موزع تشخيصي كبير بسبب نقص وثائق CE.
- رفضت وكالة شراء مستشفى فرنسية شحنة لأن تعليمات الاستخدام كانت بالصينية والإنجليزية فقط.
- غُرّم مستورد مقيم في المملكة المتحدة (قبل بريكست) لعدم التسجيل في EUDAMED بعد استيراد أجهزة من الفئة IIa.
كيفية التقدم في عام 2025
- العمل فقط مع مصنعين موثوقين مثل هانهنغ ذوي خبرة مثبتة في الامتثال الأوروبي
- إجراء تدقيق قائمة التحقق قبل الشحن لكل طلب
- استخدام وكيل استيراد أو وسيط جمركي على دراية ببروتوكولات الأجهزة الطبية
- الاشتراك في التحديثات من قطاع الأجهزة الطبية في المفوضية الأوروبية
- توثيق كل مرحلة من مراحل الاستيراد والتوزيع
قائمة التحقق من الامتثال لمستوردي الاتحاد الأوروبي
✅ التحقق من علامة CE وتوافق MDR
✅ التأكيد على تعيين وتسجيل ممثل مصرح له في الاتحاد الأوروبي
✅ مراجعة وأرشفة جميع الوثائق الفنية
✅ التأكد من أن التسميات وتعليمات الاستخدام تلبي المتطلبات اللغوية والقانونية
✅ تسجيل الجهاز والمشغل في EUDAMED
✅ مراقبة الأداء بعد السوق وتقارير الحوادث
الاستباقية—وليس التفاعل—هي المفتاح للعمليات طويلة الأمد الناجحة في سوق المستلزمات الطبية في الاتحاد الأوروبي.
9. أسئلة شائعة: التنقل في قواعد الاستيراد الأوروبية للمسحات الطبية
فيما يلي الأسئلة الأكثر تداولاً من مشتري B2B والمستوردين والموزعين الطبيين بشأن استيراد المسحات إلى الاتحاد الأوروبي في عام 2025.
س1: هل تتطلب جميع المسحات الطبية علامة CE؟
نعم. إذا كانت المسحة مخصصة للاستخدام الطبي أو التشخيصي (مثل مسحات الأنف الحلقي أو فرش الرحم)، فيجب أن تكون معلمة بعلامة CE بموجب MDR 2017/745.
س2: ما هي الفئة للمسحات الطبية بموجب MDR؟
- مسحات الأنف/الحلق: الفئة I
- فرش/كاشطات الرحم: الفئة IIa
- مجموعات الاستعلام الذاتي: قد تختلف لكنها غالباً الفئة IIa
تحقق دائماً من الاستخدام المقصود واستشر تبرير تصنيف الشركة المصنعة.
س3: ما هي الوثائق التي يجب طلبها من مورد مثل هانهنغ؟
- إعلان المطابقة
- شهادة CE (إذا كانت الفئة IIa)
- الملف الفني (الملحق II)
- تقارير التعقيم
- شهادات ISO13485 وISO9001
- تعليمات الاستخدام والتسمية بلغات الاتحاد الأوروبي
س4: هل يمكنني استيراد المسحات دون ممثل مصرح به في الاتحاد الأوروبي؟
لا. إذا كانت الشركة المصنعة خارج الاتحاد الأوروبي، فإن تعيين ممثل مصرح به أمر إلزامي.
س5: هل تقدم هانهنغ دعماً للامتثال لاستيراد الاتحاد الأوروبي؟
نعم. تقدم هانهنغ وثائق كاملة متوافقة مع اللائحة MDR، ومنتجات تحمل علامة CE، ويمكنها التوصية بممثلين مصرح بهم في الاتحاد الأوروبي وشركاء لوجستيين ذوي خبرة في استيراد الأجهزة الطبية.
س6: هل هناك رسوم جمركية على المسحات الطبية؟
قد تكون المسحات الطبية مؤهلة لرسوم جمركية مخفضة أو إعفاءات بموجب رموز TARIC معينة. ومع ذلك، ستظل ضريبة القيمة المضافة على الاستيراد سارية اعتماداً على الدولة.
س7: هل يمكنني وضع علامة تجارية خاصة على منتجات هانهنغ لعلامتي التجارية في الاتحاد الأوروبي؟
نعم، تقدم هانهنغ خدمات OEM/الوضع التجاري الخاص مع وثائق متوافقة مع CE، مما يجعلها مثالية للموزعين الراغبين في التوسع تحت علامتهم التجارية الخاصة.
س8: كيف أضمن تسجيل منتجاتي في نظام EUDAMED؟
نسق مع الشركة المصنعة والممثل المصرح به في الاتحاد الأوروبي لضمان تسجيل الـ Basic UDI-DI وسرد المنتج في نظام EUDAMED.
🧪 جاهز لبناء سلسلة توريد متوافقة مع الاتحاد الأوروبي للمسحات الطبية؟
Jiangsu Hanheng Medical Technology هو شريكك الموثوق للمواد الاستهلاكية عالية الأداء المعتمدة بشهادة CE. اتصل بنا اليوم للحصول على عرض أسعار، أو مراجعة الوثائق، أو استشارة في الامتثال:
🌐 الموقع الإلكتروني: www.hanheng-medical.com
📧 البريد الإلكتروني [email protected]
ابدأ الاستيراد بذكاء وأمان أكبر مع هانهنغ — الرائد العالمي في تصنيع المسحات الطبية لأسواق الاتحاد الأوروبي.

Jiangsu Hanheng Medical Technology Co., Ltd.
نحن شركة رائدة في مجال تصنيع المواد الاستهلاكية الطبية عالية الجودة، ملتزمون بالدقة والسلامة والامتثال العالمي. ومن خلال تكنولوجيا الإنتاج المتقدمة، والرقابة الصارمة على الجودة، وفريق البحث والتطوير المتخصص، نقدم حلولاً موثوقة مصممة خصيصاً لتلبية الاحتياجات المتطورة لصناعة الرعاية الصحية.